Pengecatan Ziehl Neelsen (ZN)
Farida Juliantina R dan Irena Agustiningtyas
Capaian Pembelajaran
Setelah mempelajari bab ini mahasiswa dapat :
- Menjelaskan tujuan pemeriksaan Ziehl Neelson (ZN)
- Menjelaskan prinsip pengecatan ZN
- Menjelaskan pengambilan sampel untuk pengecatan ZN
- Menjelaskan penulisan identitas untuk pengecatan ZN
- Menjelaskan prosedur pengecatan ZN
- Menejlaskan kualitas sediaan untuk pengecatan ZN
Pendahuluan
Pewarnaan (pengecatan) Ziehl-Neelsen (ZN), disebut juga dikenali sebagai pewarna bakteri tahan asam atau sering disebut pengecatan BTA. Dalam cat ini mengandung zat warna karbol-fuchsin yang merupakan asam. Pengecatan ini pertama sekali dicetuskan oleh dua orang doktor Jerman, Franz Ziehl (1859-1926), seorang pakar bakteria dan Friedrich Neelsen (1854-1894), ahli patologi. Pengecatan ZN merupakan pewarna bakteri khas yang digunakan untuk organisme/bakteri tahan asam, terutamanya Mycobacteria.
Mycobacterium tuberculosis adalah yang paling penting dalam kumpulan ini, yang merupakan penyebab tuberkulosis (TB). Mycobacterium tuberculosis dindingnya banyak mengandung lipid sehingga sulit terwarnai oleh pengecatan Gram. Pemeriksaan ZN merupakan pemeriksaan sederhana untuk mengidentifikasi adanya Mycobacterium tuberculosis atau BTA di dalam sediaan. Pengecatan ini juga dapat digunakan untuk mendeteksi keberadaan Mycobacterium lepra yang merupakan penyebab penyakit lepra dan juga mikobakteria lain.
Tujuan pemeriksaan ZN
- Pemeriksaan ZN pada pasien yang diduga terinfeksi Mycobacterium tuberculose yang
menyebabkan tuberkulosis. Infeksi oleh bakteri ini dilakukan dengan pemeriksaan
sputum sewaktu-pagi-sewaktu (S-P-S) sebelum kemudian dilakukan pemeriksaan kultur. Diagnosis standar untuk menegakkan tuberkulosis adalah dengan kultur, biasanya dari sputum. Pemeriksaan kultur membutuhkan waktu lama yaitu 6 bulan atau lebih. Bakteri ini dapat ditumbuhkan pada media kultur sebagai berikut:
-
- Egg base media : Lowenstein Jensen
- Agar base media : Middle brook

Gambar 1. Media Lowenstein Jensen
- Pemeriksaan ZN pada pasien yang diduga terinfeksi Mycobacterium leprae. Bakteri ini menyebabkan penyakit kulit yang disebut sebagai lepra atau morbus Hansen. Slit skin smear atau skin smear merupakan pemeriksaan kerokan jaringan kulit dengan cara insisi dan kerokan kulit. Hasil dari apusan kulit (slit–skin smear) digunakan untuk diagnosis dan prognosis dari lepra. Diagnosis lepra minimal memenuhi 1 dari 3 tanda kardinal yaitu (WHO, 2018) :
- Kehilangan sensasi pada lesi yang mengalami hipopigmentasi
- Penebalan saraf perifer disertai dengan kehilangan sensasi dan kelemahan otot
pada saraf terkait
- Didapatkan bakteri tahan asam pada pemeriksaan skin-slit smear
Apusan kulit ini merupakan prosedur invasif, sehingga diperlukan tindakan yang aseptik. Spesimen diambil dari lobules kedua telinga, salah satu lesi
hipopigmentasi.
Prinsip pengecatan ZN
Mycobacterium sp memiliki dinding sel yang tebal mengandung wax dari lipid dan asam mikolat yang menyebabkan bakteri ini sulit ditembus oleh pengecatan biasa. Komposisi cat ZN dan mekanisme pengecatan ZN
Komposisi cat ZN
- ZN A: cat primer, berisi Carbol fuchsin 1%, cat merah gelap dalam 5% phenol yang larut dalam bahan lipid seperti yang dimiliki oleh dinding sel Mycobacterium sp. Penetrasi cat ini akan dipermudah dengan adanya pemanasan yang membantu carbol fuchsin menembus dinding lipid menuju sitoplasma.
- ZN B: decolorizing agent, berisi asam alkohol (3% HCl dan 95% Ethanol). Sifat larutan ini mampu mengeraskan dinding sel yang tersusun dari lipid. Dekolorisasi menggunakan asam alkohol tidak dapat melunturkan cat primer (ZN A), karena ZN
A lebih larut dibandingkan ZN B. ZN A tertahan di dalam sitoplasma, yang menyebabkan bakteri ini tetap berwarna merah.
- ZN C: counterstain, berisi Methylene blue 0,1%. Hanya sel bakteri non-BTA yang terwarnai oleh methylene blue karena mengalami dekolorisasi pada saat pencucian dengan ZN B. Sedangkan bakteri Mycobacterium sp. yang merupakan BTA telah meretensi cat ZN A.
Tuberculosis (Kemenkes RI, 2012)
-
-
- Pengambilan spesimen pada tuberkulosis
-
Pengambilan sputum dilakukan selama 2 hari berturut-turut, yaitu: Sewaktu-
Pagi-Sewaktu.
-
-
-
- Sewaktu hari-1 (A)
-
-
Pasien mengumpulkan sputum saat kunjungan pertama. Pasien dibawakan pot sputum untuk dibawa pulang.
-
-
-
- Pagi hari-2 (B)
-
-
Sputum pasien dikumpulkan pada pagi hari setelah bangun tidur dibawa kemudian dibawa ke laboratorium.
-
-
-
- Sewaktu hari-2 (C)
-
-
Saat membawa sputum hari kedua ke laboratorium, pasien mengumpulkan dahak kembali (sewaktu).
-
-
- Penulisan identitas (Kemenkes, 2017)
-
Pengisian formulir TB 05 adalah formulir yang diberikan oleh petugas di bagian pemeriksaan sebagai pengantar pasien ke laboratorium pemeriksaan dahak. Terapat nomor identitas dengan penulisan mengikuti aturan :
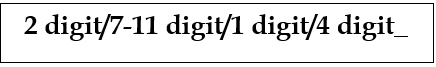
Gambar 2. Penulisan identitas pemeriksaan tuberkulosis
Keterangan:
- 2 digit = tahun berjalan pengambiland ahak
- 7-11 digit = 7 untuk RS, 11 untuk Puskesmas
- 1 digit = angka 1 untuk terduga TB SO (sensitif obat), angka 2 untuk terduga TB RO (resisten obat)
- 4 digit = no urut terduga TB dan terduga RO sesuai register TB. 06
- “_” = kode huruf sesuai waktu pengambilan dahak
Sedangkan penulisan nomor identitas kaca sediaan di bagian frosted adalah sebagai berikut: 1 digit/4 digit_

Gambar 3. Identitas sediaan BTA
-
-
- Alat dan bahan
- Spesimen dahak
- Kaca obyek
- Lidi pipih/geprek
- Lidi lancip
- Pensil 2B
- Plastik berisi disinfektan
- Bunsen dan korek
- Cat ZN A (Carbol fuchsin 1%) , ZN B (Asam alkohol 3%), dan ZN C (Methylen blue 0,1%)
- Pinset
- Rak pengecatan
- Kertas tissue
- Alat dan bahan
-

Gambar 4. Lidi pipih/geprek dan tempat pembuangan dilapisi plastik berisi disinfektan
-
-
- Prosedur pengecatan ZN
- Cara pembuatan preparat dari sputum (dahak)
- Membersihkan kaca obyek dari kotoran dan lemak
- Menuliskan identitas pada bagian frosted dengan menggunakan pensil 2B
- Membuat apusan dengan cara mengambil sputum (dahak) yang purulent
- Cara pembuatan preparat dari sputum (dahak)
- Prosedur pengecatan ZN
-
menggunakan lidi pipih dan membuat ukuran 2×3 cm (oval)
-
-
-
-
- Meratakan apusan dahak dengan menggunakan lidi kecil dengan gerakan spiral (coil type) dan merata
- Lidi yang telah digunakan dibuang ke dalam tempat dilapisi plastik yang
-
-
-
berisi disinfektan
-
-
-
- Pengeringan
- Dibiarkan di suhu kamar
- Jika sediaan sudah kering, tidak diperbolehkan membuat gerakan spiral kembali karena berisiko aerosol
- Fiksasi
- Setelah dibuat apusan spesimen dan fiksasi
- Jepit dengan menggunakan pinset
- Lewatkan sediaan di atas api bunsen biru sebanyak 2-3 kali selama 1-2 detik. Jika dipanaskan terlalu lama dapat menyebabkan sediaan rusak.
- Pewarnaan
- Genangi sediaan dengan cat ZN A, panaskan di atas rak pengecatan dengan menggunakan api bunsen. Pemanasan sampai muncul uap dan tidak diperbolehkan sampai mendidih karena akan menimbulkan endapan kristal
- Dinginkan sekitar 10 menit
- Buang sisa Carbol fuchsin, bilas dengan air mengalir. Usahakan tidak tepat di atas spesimen
- Genangi dengan ZN B (asam alkohol) selama 10-20 detik sampai warna merah hilang (pucat)
- Bilas dengan air mengalir
- Genangi dengan cat ZN C, biarkan selama 1 menit
- Buang sisa cat ZN C, bilas dengan air mengalir.
- Keringkan sediaan pada rak pengering
- Pembacaan
- Lihat di bawah mikroskop dari dengan menggunakan lensa obyektif perbesaran 10x untuk menentukan fokus dan lapang pandang, kemudian
- Pengeringan
-
-
perbesaran lendsa obyektif 100x dengan menambahkan minyak imersi.
-
-
-
-
- Pembacaan dilakukan di sepanjang garis horizontal terpanjang dari ujung kiri ke kanan atau sebaliknya. minimal 100 lapang pandang.
- BTA akan tampak sebagai bakteri berbentuk batang berwarna merah baik soliter maupun berkelompok.
-
-
-
Gambar 5. Pembacaan BTA
-
-
- Kualitas sediaan
-
Kualitas sediaan apusan sputum BTA yang baik harus memenuhi 6 kualitas sebelum dilakukan pembacaan menggunakan tabel IUTLD. Kualitas tersebut
meliputi:
-
-
-
- Kualitas sputum
-
-
Sputum untuk pengecatan Ziehl Neelsen dikatakan baik jika pada pemeriksaan mikroskopis dengan perbesaran 10×10 ditemukan leukosit PMN ≥
25 per lapang pandang. Sputum yang baik untuk diperiksa sebaiknya yang
purulent. Berikut sputum yang dilihat di bagian bawah dari pot sediaan.
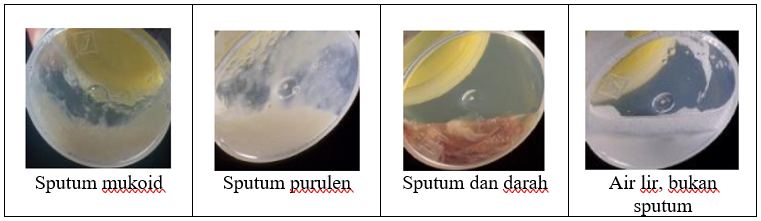
Gambar 6. Sputum pemeriksaan BTA
-
-
-
- Ukuran sediaan
-
-
Sediaan dibuat di atas glass obyek dengan ukuran 3×2 cm. Sediaan ini dibuat dengan cara mengusap dahak secara spiral hingga membentuk oval sesuai
ukuran. Dapat juga dilakukan dengan cara membuat oval menggunakan spidol di sebalik glass obyek terlebih dahulu.
-
-
-
- Ketebalan sediaan
-
-
Setelah dilakukan usapan dahak pada glass obyek selanjutnya dilakukan penilaian ketebalan. Cara ini dilakukan dengan cara meletakkan kertas bertulis di belakang glass obyek dengan jarak ± 4 cm. Penilaian ketebalan sediaan dikatakan baik jika kertas tulis masih nampak namun tidak bisa terbaca jelas.
Sediaan dikatakan ketebalannya kurang baik jika terlalu tebal atau terlalu tipis. Terlalu tebaljika kertas di belakang glass obyek tidak dapat dibaca. Dikatakan terlalu tipis jika kertas di belakang glass obyek masih dapat terbaca dengan jelas. Ketebalan dapat juga dinilai setelah dilakukan pewarnaan. Baik jika leukosit tampak tidak saling tumang tindih.

Gambar 7. Ketebalan sediaan BTA
-
-
-
- Kerataan
-
-
Penilain secara makroskopis dikatakan baik jika sediaan tampak rata, tidak ada
ruang kosong. Jika dinilai secara mikrokopis maka setiap lapang pandang akan tampak apusan dahak tersebar merata.
-
-
-
- Pewarnaan
-
-
Sediaan yang baik dari hasil pengecatan ZN akan ditunjukkan dengan adanya kontras antara BTA dengan warna latar. Jika warna latar yang mengandung Methylene blue pemberiannya terlalu lama, maka sediaan akan tampak bewarna dominan biru.
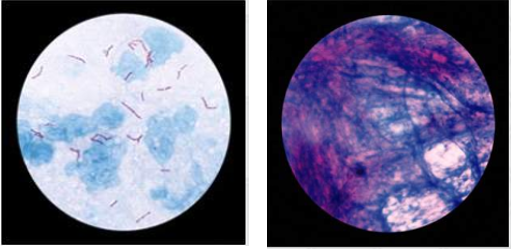
Gambar 8. Hasil pewarnaan yang baik dan yang tidak baik
-
-
-
- Kebersihan
-
-
Sediaan dikatakan bersih jika tidak emngandung cat warna siswa atau tidak
mengandung endapan kristal dari cat. Sediaan yang bersih akan memudahkan pembacaan secara mikroskopis.
-
-
- Interpretasi pengecatan ZN
-
Pembacaan hasil pemeriksaan ZN menggunakan skala International Union Against Tuberculosis Lung Diseases (IUTLD) sebagai berikut:
Tabel 1. Skala International Union Against Tuberculosis Lung Diseases (IUTLD)

Lepra (Morbus Hansen) (WHO, 2018)
-
-
- Pengambilan spesimen pada lepra dapat diambil dilakukan pada:
- Kedua cuping telinga
- Lesi aktif hipopigmentasi
- Alat dan bahan
- Bunsen dan korek
- Scalpel
- Pensil 2B
- Surgical blade steril No. 15
- Kaca obyek
- Kapas bulat steril
- Kapas lidi steril
- Kapas alkohol
- Persiapan slide
- Membersihkan kaca obyek dari kotoran dan lemak.
- Menuliskan identitas pada bagian frosted dengan menggunakan pensil 2B.
- Kaca obyek dipanaskan di atas api bunsen secara perlahan untuk
- Pengambilan spesimen pada lepra dapat diambil dilakukan pada:
-
membersihkan dari kotoran dan lemak, hindari menggunakan kertas tisu.
-
-
-
- Pasang surgical blade No. 15 pada skalpel, dan hindari menyentuh mata pisau.
- Cara pengambilan sampel (P2PL, 2012)
- Area yang akan diperiksa dibersihkan dengan menggunakan kapas alkohol
-
-
dan biarkan mengering.
-
-
-
- Pegang area dengan cara mencubit menggunakan jari jempol dan telunjuk tangan kiri. Hal ini dilakukan untuk menjauhkan darah dari tempat yang akan diperiksa serta meminimalkan perdarahan.
- Dengan menggunakan ujung mata pisau, lakukan insisi dengan ukuran 5 mm dan kedalaman 2-3 mm. Kulit tetap dicubit agar tidak terjadi perdarahan.
- Kerok bagian dasar dari celah untuk mendapatkan bahan apusan.
- Letakkan sampel pada kaca obyek dan buat apusan yang tipis dan ketebalan
-
-
yang sama dengan diameter berukuran 5-8 mm.
-
-
-
- Tekan area tempat pengambilan sampel dengan menggunakan bola kapas
-
-
steril dan hapus dengan kapas alkohol.
-
-
-
- Hapus kotoran pada scalpel dengan menggunakan kapas alcohol. Panaskan
-
-
scalpel di atas api Bunsen selama 3-4 menit. Biarkan dingin, dan hindari menyentuh sesuatu.
-
-
-
- Ulangi langkah pengambilan sampel di area yang lain.
-
-
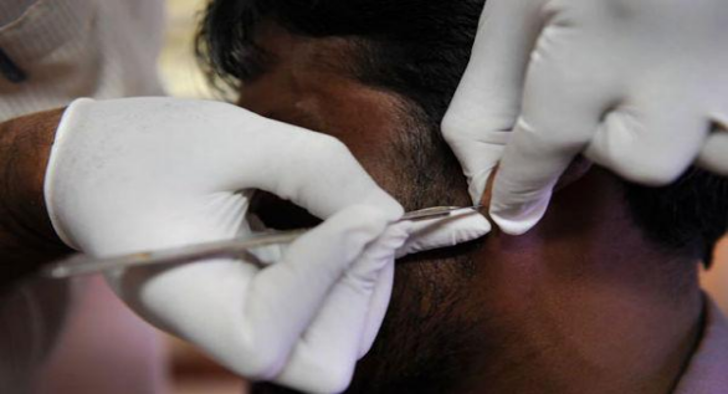
Gambar 9. Pengambilan sampel pada lobules telinga (Ali, et al, 2014)
-
-
- Fiksasi
- Dibiarkan di suhu kamar.
- Lewatkan sediaan di atas api bunsen biru sebanyak 2-3 kali selama 1-2 detik.
- Fiksasi
-
Jika dipanaskan terlalu lama dapat menyebabkan sediaan rusak. Jika terlalu
cepat dipanaskan dapat menyebabkan spesimen tidak menempel dengan baik dan mudah tercuci.
-
-
- Pewarnaan
- Letakkan kaca obyek di atas rak pengecatan.
- Genangi sediaan dengan cat ZN A (carbol fuchsin 0,3%), panaskan di atas rak pengecatan dengan menggunakan api bunsen. Pemanasan sampai muncul uap dan tidak diperbolehkan sampai mendidih karena akan menimbulkan endapan Kristal.
- Dinginkan sekitar 5 menit, namun jangan sampai mengering.
- Buang sisa Carbol fuchsin, bilas dengan air mengalir. Usahakan tidak tepat di atas spesimen.
- Genangi dengan ZN B (asam alcohol 3%) selama 5-10 detik sampai warna
- Pewarnaan
-
merah hilang (pucat)
-
-
-
- Bilas dengan air mengalir.
- Genangi dengan cat ZN C (methylene blue) sebagai counter staining, biarkan selama 1 menit.
- Buang sisa cat ZN C, bilas dengan air mengalir.
- Keringkan di atas kertas tissue, posisi berdiri miring.
- Pembacaan (WHO, 2018)
-
-
Membaca apusan slit skin smear sekitar 100 lapang pandang. Bakteri tahan asam (BTA) Mycobacterium leprae akan tampak sebagai bakteri berbentuk batang berwarna merah dengan latar belakang berwarna biru. Bentuknya dapat lurus
atau melengkung dengan warna merah merata/homogen/solid atau tidak rata/fragmented dan granular. Identifikasi BTA kemudian digunakan untuk menentukan:
-
-
-
- Indeks bakteri (IB)
-
-
Menunjukkan penilaian semikuantitatif kepadatan BTA. Tujuan pemeriksaan IB adalah untuk menentukan tipe lepra dan terapi yang sesuai. Penilaian dengan menggunakan skala logaritma Ridley.
Tabel 2. Indeks Bakteri Mycobacterium leprae

* Clumps : beberapa bentuk granuler seperti titik-titik tersusun garis lurus
atau berkelompok membentuk pulau-pulai tersendiri
-
-
-
- Indeks morfologi (IM)
-
-
Menunjukkan persentase basil lepra, bentuk utuh (solid) terhadap seluruh
BTA. Untuk mendapatkannya dicari lapang pandang yang paling baik yang tidak terdapat globus/clumps. Jika tidak ada, maka ambil lapang pandang paling sedikit mengandung globus/clamps. Jika ditemukan globus/clamps maka tidak dihitung.
IM = Jumlah BTA yang utuh x 100% Jumlah seluruh BTA
Indeks morfologi berfungsi untuk mengetahui penularan bakteri, menilai respon terhadap terapi, dan menilai adanya resistensi terhadap obat.
Hasil pengamatan

Soal diskusi
-
- Apakah tujuan pemeriksaan Ziehl Neelsen (ZN)?
- Apakah yang dimaksud dengan bakteri tahan asam?
- Bagaimana prinsip pengecatan ZN?
- Bagaimana cara pengambilan sampel [pada pasien yang dicurigai terinfeksi oleh
Mycobacterium leprae?
- Bagaimana interpretasi pembacaan mikroskopis dari BTA baik pada kasus tuberekulosis maupun lepra?
Referensi
Ali, S., Giri, V. C., Rajenderen, S. M., & Vanaja, S. G. (2014). Module for Skin Smear
Technique for GHC Lab Technician Module for Skin Smear Technique for GHC Lab Technician Module for Skin Smear Technique for GHC Lab Technician. Tamil Nadu.
Kemenkes, R. (2017). MODUL PELATIHAN LABORATORIUM TUBERKULOSIS BAGI
PETUGAS DI FASYANKES.
Kemenkes RI. (2012). Standar Prosedur Operasional Pemeriksaan Mikroskopis TB. Katalog dalam Terbitan Kemenkes RI. Panduan Bagi Petugas Laboratorium Kemenkes.
P2PL, D. (2012). Pedoman Nasional Program Penanggulangan Penyakit Kusta. WHO. (2018). Guidelines for the Diagnosis, Treatment and Prevention of Leprosy.
